近期,我校伟德国际1946官方网康振教授团队在聚合和转运胞外肝素前体产量方面取得重要进展,研究成果“Coordinated optimization of the polymerization and transportation processes to enhance the yield of exopolysaccharide heparosan”正式发表于Carbohydrate Polymers (IF =/info/1021/ /11.2) (https://doi.org/10.1016/j.carbpol.2024.121983)。
肝素(Heparin)是糖胺聚糖(Glycosaminogly cans, GAGs)家族中一类磺酸化修饰的重要酸性粘多糖。肝素在临床上主要用于治疗血栓和抗凝。传统的肝素的提取依赖于动物组织提取,主要存在产品结构不均一、纯化分离困难以及步骤繁琐等问题。相比较,肝素的生物合成受到了广泛的关注,尤其以肝素前体(Heparosan)为底物的酶法催化合成肝素取得了突破性进展。因此,构建微生物细胞工厂,实现肝素前体的高效生物合成具有重要意义。本论文围绕大肠杆菌 Nissle 1917(EcN,一株天然合成分泌肝素前体的益生菌)的肝素前体聚合、KfiB功能鉴定以及ABC(ATP-binding cassette transporter,ABC)转运系统多酶适配优化开展系统深入研究,实现肝素前体的高效合成及分泌。
康振教授团队针对优化肝素前体的生物合成和转运,从而实现有效的细胞外分布——本研究以益生菌EcN为平台菌株,首先通过蛋白共定位肝素前体合成基因簇区域II蛋白KfiB在EcN菌中的位置和生物学作用,鉴定KfiB在肝素前体生物合成中的功能,在证明了KfiB在肝素前体生物合成中的关键作用并参与肝素前体的转运过程后,进一步筛选不同强度的核糖体结合位点(ribosome binding site,RBS)重构了kfiABC基因表达盒;鉴于肝素前体在细胞内的积累,随后优化合成与转运之间的联系实现肝素前体的高效合成与转运调控,其中ABC转运蛋白KpsTM和KpsE组合优化时与KfiACB的协同上调显著促进了肝素前体的转运,使摇瓶内肝素前体浓度提高到1.03 g/L,细胞外浓度为0.96 g/L。最后,增加前体UDP-糖代谢通量、优化合成及转运组分获得的重组菌株在5-L发酵罐中放大生产,肝素前体的总产量达到12.22 g/L,分泌效率达到了91.81%,具有更高的肝素前体产率及胞外分布。结果表明,肝素前体生物合成过程中聚合与转运协同优化策略是高效可行的。该工程菌株也具有大规模生产肝素聚糖的潜力。
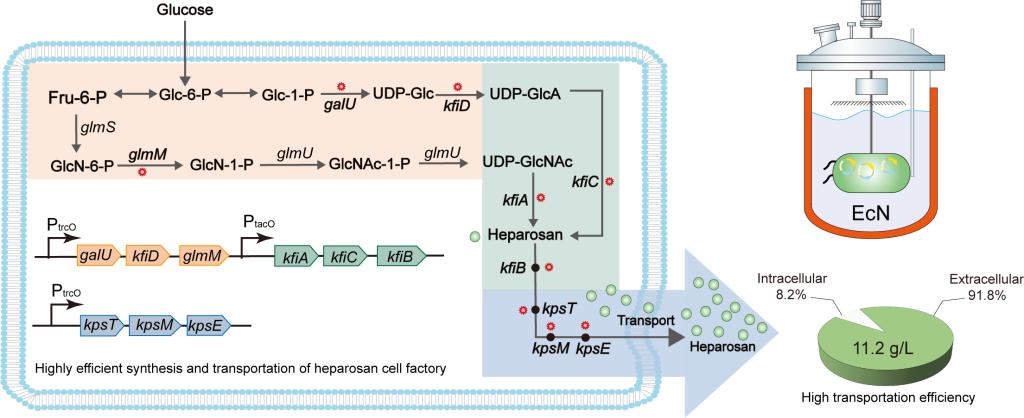
图形摘要
康振教授为论文的通讯作者,我校2019级博士生胡珊为第一作者。上述研究得到了国家重点研发计划(2018YFA0901401)、国家自然科学基金(32370066,32000058)、中央高校基本科研业务费专项资金项目(JUSRP622003)和国家轻工业技术与工程一流学科项目(QGJC20230202)等资助。
近年来康振教授团队以合成生物学科学理论为指导,在系统开展高效合成高值化合物细胞工厂构建及产业化方面取得丰硕成果,相关研究成果已发表在International Journal of Biological Macromolecules(2023)、Green Chemistry (2022)、ACS Catalysis (2021)、Nature Communication (2020)、Carbohydrate Polymers (2019)等本领域权威期刊。
